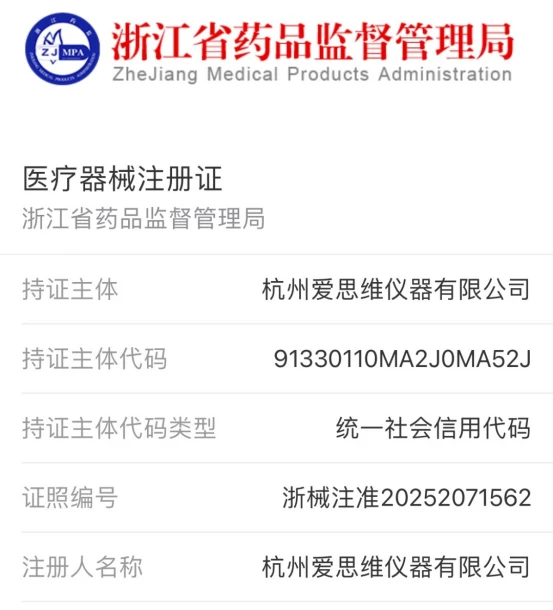
AiSW3201耳声发射听力筛查仪通过国家药品监督管理局(NMPA)审批,于2025年8月5日成功取得中华人民共和国二类医疗器械注册证,正式与用户们见面。注册证编号:浙械注准20252071562。
01 产品介绍
AiSW耳声发射听力筛查仪使用了TEOAE(瞬态声诱发耳声发射)和DPOAE(畸变产物耳声发射)技术。将一定频率、强度的声音通过探头内扬声器传入耳朵,引起耳蜗产生自主的耳声发射释放入外耳道,被探头内麦克风检测和记录,通过测量分析,最终反映耳蜗功能、状态是否正常,从而达到听力筛查的作用。

02 临床支持
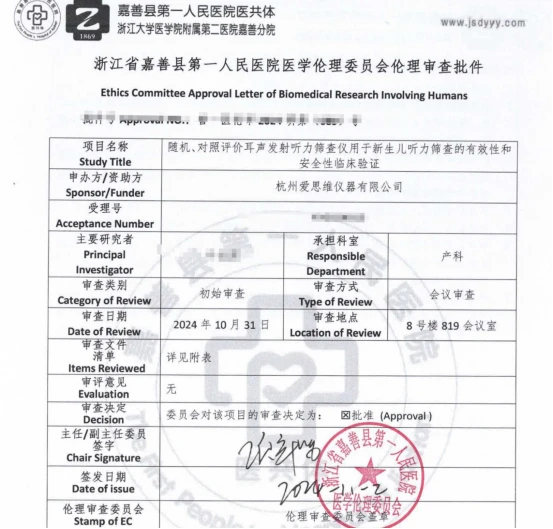
杭州爱思维仪器有限公司与浙江省xx医院合作开展了“随机、对照评价耳声发射听力筛查仪用于新生儿听力筛查的有效性和安全性临床验证”实验项目,为AiSW3201提供了更充分的临床数据支持。
□试验时间
2024年12月03日--2025年01月04日
□临床试验机构
浙江省嘉善县第一人民医院--产科
□试验设计
受试者:100名新生儿,孕期为36周~41周(早产儿10例,足月儿90例),体重为2130g~4350g(低体重儿4例,正常体重儿96例)。
方法:试验器械与对照器械(同类已上市医疗器械产品)测试相同的受试者。
□试验结果
100例受试者中,试验器械与对照器械检测结果的一致性达到了99%。
□结论
100例临床试验的试验结果表明,AiSW3201型号的耳声发射听力筛查仪适用于新生儿听力筛查以及出生48~72小时的新生儿人群,其测量性能与同 类已上市产品有很好的一致性,满足临床应用的要求,且测量对于人体是安全的。

03 功能特点
双重检测技术:TEOAE和DPOAE技术结合,提高筛查准确性
3.5寸触摸显示屏:3.5寸电容式触摸液晶显示屏,操作直观,界面友好
数据存储:测试数据自动保存,便于长期跟踪与管理
直观的图表展示:测试结果以图表形式呈现,易于理解和分析
智能结果分析:智能系统自动判定测试结果,减少人为误差
自定义注释功能:允许用户添加备注,记录特殊情况
支持外连打印机:快速打印测试结果,方便存档与分享
大容量内存:支持大量数据存储,满足长期使用需求
内置可充电锂电池:续航时间长达8小时,适合移动筛查环境
轻巧便携设计:便于在不同场景中使用,如医院、诊所、学校及家庭等
04 适用场景
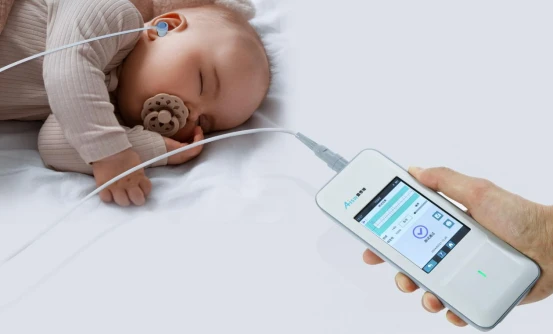
AiSW3201耳声发射听力筛查仪体积小巧便携,支持筛查型TEOAE和DPOAE,适用于新生儿听力筛查以及不同场景下的婴幼儿、成人的初步听力评估。
05 标准与认证
国际标准:符合IEC 60645-6:2022《电声学 测听设备 第6部分:耳声发射的测量仪器》2型(筛查)标准。
国家校准规范:满足JJF 1289-2020《耳声发射听力筛查仪校准规范》中2型设备的技术要求。
安全标准:符合GB 9706.1-2020《医用电气设备 第1部分:安全通用要求》的要求,确保使用安全。
电磁兼容性:符合YY 9706.102-2021及GB/T7341.1-2010的要求,保证设备的电磁兼容性能。